卡格列净对糖尿病视网膜病变治疗效果的网络药理学分析

王昀 寿悦颖 李金洋 教莹莹 孙兆义 金丽娇 卫冬
牡丹江医科大学附属红旗医院 黑龙江省牡丹江 157011 牡丹江医科大学 黑龙江省牡丹江 157011
1 前言
糖尿病视网膜病变(DR)是糖尿病患者常见的慢性并发症之一,该病是 20-74 岁的成年人视力丧失的主要原因 [1]。DR 对糖尿病患者的生活质量构成严重威胁,同时也给社会带来巨大的经济负担。不可逆的 DR 导致病人早期往往缺乏明显的自觉症状,确诊糖尿病后,应积极地控糖、控脂并定期参与 DR 的筛查,以期延缓其出现的时间;而当糖尿病患者确诊 DR 并已发生视力损伤时,目前的治疗手段仅能减缓其进展,保存患者的残存视力,无法恢复已经受损的视力。因此,开发毒副作用小且有效的早期防治DR 的药物成为当前的急需。
最近研究表明 [2],SGLT2 在视网膜微循环系统中可能承担功能性葡萄糖感受器作用,通过感受细胞外葡萄糖浓度调节视周细胞的张力。当细胞外葡萄糖浓度升高时,SGLT2i 通过抑制周细胞上 SGLT2 表达,减少高糖在视网膜周细胞的聚集,从而降低葡萄糖毒性,起到抗炎、抗氧化以及保护视周细胞作用。虽然SGLT2i 治疗DR 的作用得到证实,但其具体的作用机制还需进一步研究。
网络药理学是一门新兴的交叉学科,它结合了数学、计算机科学和网络科学等多学科的方法,系统、科学、全面地探索药物治疗疾病的潜在分子机制。因此,本研究拟采用网络药理学分析卡格列净和DR 作用靶点和通路等信息为卡格列净对糖 DR 作用机制的理解提供科学依据。
2 材料与方法
2.1 预测卡格列净和 DR 相关作用靶点
通过ChemicalBook 数据库,获得卡格列净的化学物质登录(CAS)编号(CAS:842133-18-0)。从 PubChem 数据库下载了卡格列净的规范化简系统方程式(SMILES)字符串以及其二维结构,并以结构数据文件(SDF)格式保存。利用 UniProt 数据库将卡格列净的信息转换为目标基因。从 PubChem 数据库获取了卡格列净的 SDF 分子结构,并将其输入到 PharmMapper 数据库中,以获取卡格列净的潜在靶点。通过输入卡格列净的 SMILES 字符串到 SwissTargetPrediction 数据库,获取了卡格列净的相关靶点。此外,还使用了比较毒物学数据库(CTD)和 SuperPred 数据库进行补充,并对获取到的靶点信息进行了整合和去重。然后,使用关键词“diabetic retinopathy”在 GeneCards 数据库,Online Mendelian Inheritance in Man (OMIM)数据库,DrugBank 数据库,以及CTD 数据库中搜索DR 的相关靶点,并对获取到的靶点信息进行了去重和整理。
2.2 确定卡格列净治疗 DR 共同靶点
我们使用了 EVenn 在线工具来确定卡格列净和 DR 相关靶点的交集。这些交集靶点被认为是卡格列净治疗DR 的共享靶点。
2.3 构建卡格列净治疗 DR 核心靶点的蛋白质 - 蛋白质相互作用(PPI)网络
将 2.2 节中获取的靶点输入到 STRING 分析平台中以构建蛋白质互作网络,将物种设定为“Homo Sapiens”,并将最高置信度设置为>0.4 。我们隐藏了网络中的孤立节点,并使用 Cytoscape 3.10.0 软件将靶点互作关系进行可视化处理。通过 Network Analyzer、CytoHubba 插件和 MCODE 插件,我们分析了网络中节点的拓扑参数,绘制 PPI 网络图并获取核心靶点。
2.4 对卡格列净治疗 DR 核心靶点 GO 分析和 KEGG 通路富集分析
将 2.3 中获取的核心靶点输入到 DAVID 数据库中,并设定为“Official Gene Symbol,Homo Sapiens”。选择 Gene Ontology 中的生物过程 BP、CC、MF 以及 Pathway 中的 KEGG 通路,设定显著性 P<0.05 ,以获取显著富集的 GO 生物过程和信号通路。将结果导入微生信在线作图平台,分别以富集圆圈图、双 X 轴 bar 线图和气泡图的形式展示GO 功能富集分析结果和KEGG 通路富集分析结果。
3 结果
3.1 卡格列净靶点及 DR 靶点的筛选
在进行了数据库查询并筛选后,共筛选出 506 个与卡格列净作用相关的靶点。通过深入分析 GeneCards、OMIM 等数据库,并进行去重和相关性筛选,确定了 5244 个与 DR 相关的疾病靶点。进一步交叉分析药物靶点与疾病靶点后,筛选出 222 个共同靶点,这些靶点是卡格列净治疗DR 的潜在作用靶点(见图1)。
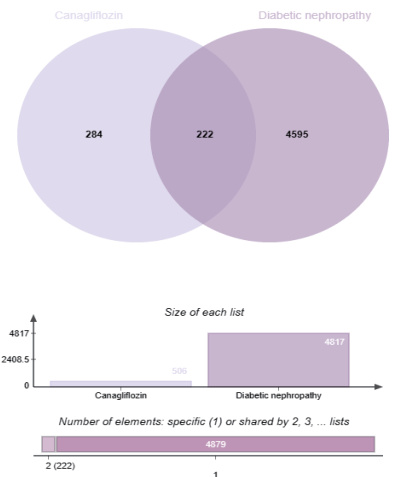
3.2 卡格列净防治 DR 交集靶点的PPI 网络及核心基因的获得
通过将筛选出的交集靶点导入 STRING 网络分析平台,生成 TSV文件,并将其导入 Cytoscape 3.10.1 软件,构建了 PPI 网络。该网络包含 214 个节点和 2958 条边。使用 CytoHubba 插件并基于 Degree 算法,筛选出得分排名前 10 的核心基因,并进行了可视化展示,如图 2A所示。利用 MCODE 插件分析 PPI 网络中的关键模块,共识别出 6 个Cluster 模块。由于最后一个Cluster 的节点数量少于4,未进行可视化展示,仅展示了5 个Cluster,详见图 2B。
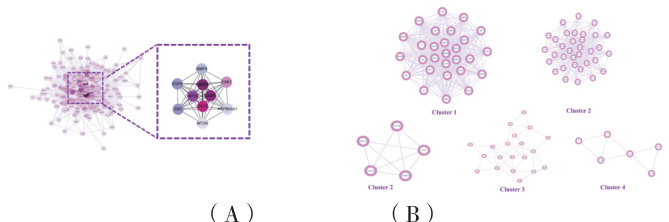
3.3 GO 和 KEGG 富集分析
通过 DAVID 数据库对 222 个交集靶点进行 GO 和 KEGG 富集分析。在 P<0.05 的标准下,共筛选出 442 个 GO 富集项,其中包括245 个 BP、79 个 CC 和 118 个 MF。GO 分析揭示 BP 主要涉及 proteinphosphorylation 等;CC 主要涉及 extracellular exosome、cytosol 等;MF则主要涉及 protein serine/threonine/tyrosine kinase activity 等。通过富集圆圈图展示了 BP、CC、MF 中排名前 8 的条目,见图 3A。在 KEGG富集分析中,共鉴定到 157 条通路,包括 Prostate cancer、Pathways incancer、Central carbon metabolism in cancer 等(见图 3B)。在卡格列净治疗DR 的通路机制中,可能与PI3K-Akt 信号通路、HIF-1 信号通路、AGE-RAGE 信号通路等相关。根据 P 值对富集结果进行排序,并绘制了相应的气泡图(图3C、图 3D)。
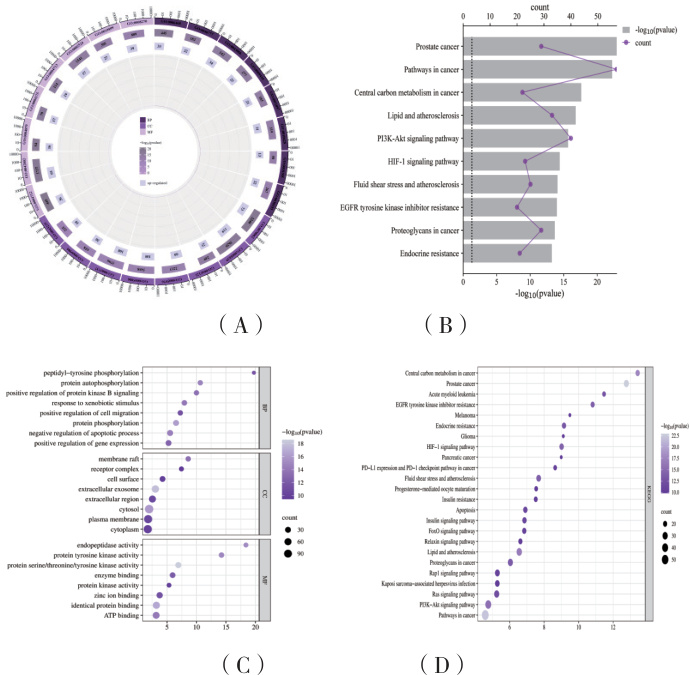
4 讨论
随着糖尿病患者群体的年轻化和普及化趋势,DR 逐渐成为严重威胁公众视力健康的主要因素。DR 作为一种典型的糖尿病微血管并发症,其特点在于视网膜血管病变的发生远早于临床症状的出现,这一特点强调了早期预防和干预 DR 的重要性。病理学研究揭示,DR的关键组织学变化之一是视网膜微血管周围细胞的丢失,这导致血 -视网膜屏障(BRB)功能的永久性损害。尽管目前的药物治疗可以缓解症状并减缓疾病进展,但尚无法彻底治愈 DR,因此,探索有效的早期治疗策略成为一大挑战。
卡格列净作为 SGLT2 抑制剂的研究中,其通过特异性抑制肾小管上皮细胞中的 SGLT2,减少肾脏对葡萄糖的重吸收,从而促进尿糖排泄,达到降低血糖水平的效果。长期的高血糖状态是糖尿病微血管损伤的主要原因,而 DR 的发展与糖尿病微血管并发症有着直接关联[3,4]。从这一机制来讲,卡格列净可能通过抗炎、抗氧化应激、调节内皮细胞存活、影响细胞因子表达、抑制细胞凋亡以及增加血管反应性等多种机制来改善 DR。在本研究中,通过整合 GeneCards、OMIM、DrugBank 和 CTD 等数据库,我们筛选出了 5244 个与 DR 相关的基因,以及506 个卡格列净的靶点基因。进一步地,通过取这些基因的交集,我们确定了 222 个药物 - 疾病共同靶点。通过 GO 富集分析,我们揭示了与 DR 治疗相关的关键生物过程,包括氧化应激反应、细胞内氧化调控、转录因子及其相关受体活性的调控等。此外,高糖环境还可诱导 NF-κB 的活化,进而增加视网膜血管内皮细胞中的 ROS,促进内皮细胞凋亡 [5,7]。这些发现表明,活性氧的增加是导致 DR 的一个重要原因。因此,本次 GO 富集分析的结果表明卡格列净对 DR 的治疗作用可能涉及多个生物过程的同时调节。
在本研究的 KEGG 通路富集分析中,我们发现了多个与 DR 密切相关的信号通路。其中,HIF-1 信号通路的活化是对低氧状态的适应性反应,关键分子为低氧诱导因子 -1α ( HIF-1α )。HIF-1 通路的激活可促进细胞内多种基因的表达,涉及代谢反应、血管新生、细胞增殖与存活,以及在某些情况下诱导细胞凋亡[6]。除此之外,Akt 的活化还可以激活 NF-κB 信号通路,该通路与多种炎症因子的表达紧密相关[7]。抑制 NF
综合以上研究成果,我们认为卡格列净通过影响多个信号通路,尤其是 AGE-RAGE、PI3K-Akt 等通路,有可能在调控 DR 中发挥重要作用。这对于糖尿病并发症的治疗提供了新的视角和治疗策略。
参考文献:
[1]CHEUNG N, MITCHELL P, WONG T Y. Diabetic retinopathy
[J]. Lancet, 2010, 376(9735): 124-36.
[2]Eleftheriadou A, Riley D, Zhao SS, Austin P, Hernández G, Lip
GYH, Jackson TL, Wilding JPH, Alam U. Risk of diabetic retinopathy and
diabetic macular oedema with sodium-glucose cotransporter 2 inhibitors
and glucagon-like peptide 1 receptor agonists in type 2 diabetes: a real
world data study from a global federated database. Diabetologia. 2024
Jul;67(7):1271-1282.
[3]Lin TY, Kang EY, Shao SC, Lai EC, Garg SJ, Chen KJ, Kang JH,
Wu WC, Lai CC, Hwang YS. Risk of Diabetic Retinopathy between
Sodium-Glucose Cotransporter-2 Inhibitors and Glucagon-Like
Peptide-1 Receptor Agonists. Diabetes Metab J. 2023 May;47(3):394-404.
[4]Yen FS, Wei JC, Yu TS, Hung YT, Hsu CC, Hwu CM. Sodium
Glucose Cotransporter 2 Inhibitors and Risk of Retinopathy in Patients
With Type 2 Diabetes. JAMA Netw Open. 2023 Dec 1;6(12):e2348431.
[5]Liang WJ, Yang HW, Liu HN, Qian W, Chen XL. HMGB1
upregulates 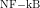 by inhibiting IKB-α and associates with diabetic
by inhibiting IKB-α and associates with diabetic
retinopathy. Life Sci. 2020 Jan 15;241:117146.
[6]Sun K, Chen Y, Zheng S, Wan W, Hu K. Genipin ameliorates
diabetic retinopathy via the HIF-1α and AGEs-RAGE pathways.
Phytomedicine. 2024 Jul;129:155596.
[7]Tang L, Zhang C, Lu L, Tian H, Liu K, Luo D, Qiu Q, Xu GT,
Zhang J. Melatonin Maintains Inner Blood-Retinal Barrier by Regulating
Microglia via Inhibition of PI3K/Akt/Stat3/NF- κ B Signaling Pathways
in Experimental Diabetic Retinopathy. Front Immunol. 2022 Mar
15;13:831660. 基 金: 黑 龙 江 省 省 属 高 等 学 校 基 本 科 研 业 务 费
2020-KYYWF-0771 第一作者:王昀(1989.11)女,汉族,市,本
科学士,。 ⋆ 通讯作者:卫冬。
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)