关于分子诊断试剂设计开发过程的关键控制点和常见问题

李弘韬
湖南宏雅基因技术有限公司 湖南长沙 410000
分子诊断试剂主要是利用分子生物学方法,对人体样本中存在的遗传物质等基因结构或者类型等进行检测,从基因的角度应对各种疾病的靶标等进行定量或者定性检测。分子诊断产品在肿瘤以及遗传病等各领域得到了合理的利用,要想保证分子诊断设计设计开发过程中,要遵循风险管理的基本原则,同时结合高新技术手段,对产品质量影响因素等进行分析,在保证产品安全的同时,实现对其质量的合理管控,以此来保证分子诊断试剂设计开发的整体质量。
1 分子诊断试剂
1.1 原理
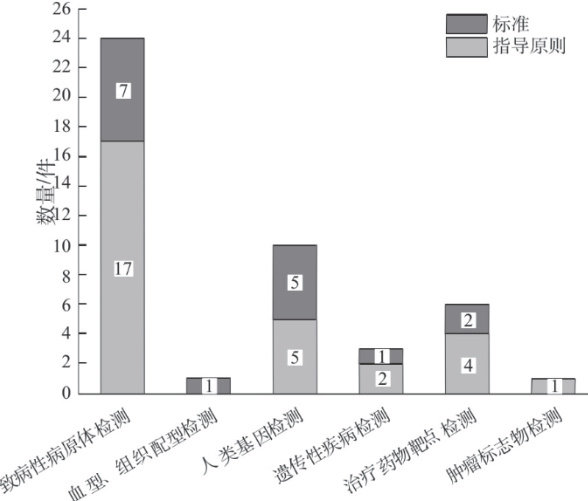
分子诊断试剂是生物化工领域中用于检测生物体内分子水平变化,从而对疾病进行诊断、监测和预后评估的一类试剂。分子诊断试剂主要基于核酸分子杂交、聚合酶链反应(PCR)、基因测序、荧光定量 PCR、基因芯片等技术,如核酸分子杂交是利用互补的核酸单链能够在一定条件下结合成双链的特性,通过标记已知序列的核酸探针来检测样本中是否存在与之互补的目标核酸序列 [1]。分子诊断试剂产品相关的标准和指导原则的数量分布,如图1 所示。
图1分子诊断试剂产品相关的标准和指导原则的数量分布
1.2 种类
1.2.1 核酸提取试剂
核酸提取试剂用于从血液、组织、细胞等各种生物样本中分离和纯化核酸,是后续分子诊断检测的基础步骤,常见的有磁珠法核酸提取试剂、硅胶膜离心柱法核酸提取试剂等。
1.2.2 PCR 试剂
PCR 试剂中包括 PCR 预混液、Taq 酶、引物、dNTP 等,其中,PCR 预混液包含了 PCR 反应所需的缓冲液、镁离子等成分,而 Taq 酶是一种热稳定的 DNA 聚合酶,能够在高温下催化 DNA 的合成[2]。此外,引物是根据目标核酸序列设计的短链DNA,决定了PCR 扩增的特异性,而dNTP 是合成DNA 的原料。
1.2.3 荧光定量 PCR 试剂
在普通 PCR 试剂的基础上,加入了荧光标记的探针或染料,常用的荧光染料如 SYBR Green I,能与双链DNA 特异性结合并发出荧光,通过实时监测荧光信号的变化, 实现对核酸模板的定量分析。荧光标记探针则具有更高的特异性,如 TaqMan 探针的两端分别标记有荧光报告基团和淬灭基团,当探针与目标核酸杂交后,Taq酶的外切酶活性会将探针切断,使报告基团与淬灭基团分离,从而产生荧光信号。
配方进行优化和验证,确定最佳成分比例,同时评估不同配方比例下试剂的稳定性,包括热稳定性、长期稳定性等。通过加速稳定性试验和长期稳定性试验,观察试剂在不同条件下的性能变化,如在不同温度、湿度条件下放置一定时间后,检测试剂的活性、准确性等指标,确定配方的稳定性。
3.2.2 反应条件控制
操作人员确控制反应温度,不同的反应步骤需要不同的温度条件,并维持反应体系的合适 pH 值,保证生物分子的活性和反应的顺利进行,不同的试剂有不同的最适 pH 范围,如某些酶促反应的 pH 值需控制在 7-8 之间,过酸或过碱都会影响酶的活性。同时还要严格控制反应时间,确保反应充分进行但不过度反应。
3.3 检验操作
3.3.1 人员要求
检验人员应具备扎实的生物化学、分子生物学等相关专业知识,熟悉分子诊断试剂的检验原理和操作技能,在上岗前需经过系统的培训,包括理论知识学习和实际操作训练,培训内容应涵盖仪器设备的操作、检验方法的原理和步骤、质量控制要求等方面。检验人员在操作过程中必须严格遵守既定的操作规程,不得随意更改操作步骤和参数,确保检验结果的准确性和可重复性。
3.3.2 仪器设备的校准与维护
对核酸扩增仪、酶标仪、离心机等用于检验的仪器设备要按照规定的周期进行校准,校准工作应由专业的计量机构或具备资质的人员进行,确保仪器的各项性能指标符合要求 [5]。还要意识到仪器设备的日常维护保养的重要性,检验人员应按照仪器的使用说明书进行日常维护,如定期清洁仪器表面、更换磨损的部件等。当仪器出现故障时,应及时记录故障现象,并通知专业维修人员进行维修。维修后需对仪器进行性能验证,合格后方可继续使用。
3.3.3 试剂和耗材的质量把控
对于采购的引物、探针、酶、微孔板等试剂和耗材要进行严格的质量验收,检查产品的包装是否完好、标签信息是否完整、有效期是否符合要求等,同时要对试剂的性能进行检测。其中试剂和耗材的保存条件应严格按照说明书要求执行,在使用过程中,要注意试剂的开启次数和使用期限,避免因保存不当或过期使用导致试剂性能下降,影响检验结果。
3.3.4 检验方法的选择与验证
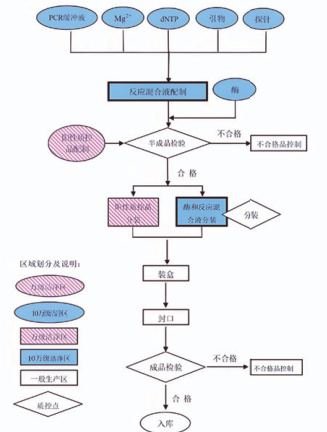
根据分子诊断试剂的特点和预期用途,选择合适的检验方法,所选方法应具有良好的特异性、灵敏度和准确性,并且经过国内外权威机构认可或广泛应用于临床实践。在使用新的检验方法前,需要进行全面的验证,验证内容包括特异性、灵敏度、精密度、准确性、线性范围等指标的评估。通过使用已知浓度的标准品、阳性和阴性样本等,对检验方法进行性能验证,确保其符合设计开发的要求。分子诊断试剂生产工艺流程图,如图2 所示。
2 分子诊断试剂设计开发现存问题
对临床实际应用场景和医生 患者的真实需求了解不足, 没有充分考虑到临床对于检测灵敏度和特异性的严格要求,开发出的试剂在临床 诊断试剂属于医疗器械范畴,受到严格的法规监管,但是目 设计开发输入的内容不符合法规要求。尤其是行业标准和技术规 用最新的标准,使试剂的设计开发输入落后于行业要求。此外,对新 ,在试剂设计中盲目应用,导致试剂性能不稳定或不准确。
2.2 设计开发输出
2.1 设计开发输入
2.2.1 产品性能方面
由于引物或探针设计不合理,与目标核酸序列的匹配度不够高,导致非特异性扩增或杂交,从而影响检测结果的准确性。同时试剂对低浓度目标物的检测能力不足,比如在肿瘤标志物的分子诊断试剂中,无法检测到早期肿瘤患者体内微量的肿瘤标志物核酸或蛋白,导致漏诊[3]。试剂在常规保存条件下容易失效,究其原因是由于试剂中的酶、抗体等生物活性成分在保存过程中容易变性失活。试剂在规定的保存条件下,能够保持其性能稳定的时间较短,主要是由于试剂的配方不合理,或者包装材料对试剂的保护作用不够。
2.2.2 生产工艺方面
不同批次生产的试剂在性能上存在较大差异,其是由于生产过程中对原材料的质量控制不严格,或者生产工艺参数的控制不够精准。同时生产工艺过于复杂,对操作人员的技能要求过高,难以保证每次生产都能达到相同的质量标准。此外,放大生产过程中,原有的工艺参数不再适用,需要重新优化和调整,但如果对工艺参数的调整不当,势必会导致试剂的性能下降。
3 分子诊断试剂设计开发过程的关键控制点
图2分子诊断试剂生产工艺流程图
3.1 主要原材料
3.1.1 生物活性物质
首先,DNA 或 RNA 等核酸可作为检测靶 也可用于制备核酸探针或引物,在基因检测试剂中,特定的DNA 片段可作为模板,通过聚合酶 要包括抗原和抗体,抗原可用于检测相应抗体,如在传染病诊断 抗体结合,通过检测这种结合来判断是否感染,而抗体则用于检测抗原 试纸条上,用于捕获样本中的目标抗原。此外,化学试剂用于维持反应体系的 和反应的正常进行,不同的分子诊断反应需要不同的缓冲液。
3.1.2 酶类
聚合酶在 PCR 技术中用于催化 DNA 的合成,以扩增目标核酸序列,还有逆转录酶,可将 RNA 逆转录为cDNA,用于 RNA 病毒检测或基因表达分析等。 同时限制性内切酶能识别并切割特定的 DNA 序列,在基因分析和克隆等方面有重要作用,可用于构建基因文库、分析基因结构等。而连接酶用于连接 DNA 片段,如在基因克隆中,将目的基因与载体连接起来,构建重组DNA 分子。
3.1.3 载体与耗材
微孔板、硝酸纤维素膜、磁珠等是其中比较常见的载体,其中微孔板常用于酶联免疫吸附试验,可同时检测多个样本,硝酸纤维素膜是免疫层析 试纸条 成部分, 用于固定抗体或抗原,而磁珠则可用于核酸提取和免疫分离等过程,通过磁场作用实现目标物质的分离和富集 ]。此外,PCR 管、离心管等反应容器主要是承载分子诊断反应,这些容器需要具备良好的密封性和化学稳定性,以防止反应液泄漏和与试剂发生化学反应。
3.2 生产工艺配方
3.2.1 确保配方比例精确性
操作人员需要精确称量和配比各成分,使用高精度的天平、移液器等计量设备,并定期校准。通过实验对
3.3.5 质量控制与结果判定
在检验过程中,应建立严格的室内质量控制体系, 定期使用标准品、质控品进行检测,监控检验结果的准确性和精密度,一旦发现质控结果超 并采取纠正措施。检验人员应根据既定的判定标准对检验结果进行 过程中明确规定,并且经过充分的验证。对于阳性和阴性结果的判定, 虑检测信号值 果等因素。在出具检验报告时,应确保报告内容准确、完整,包括样本信息、 检验 目、检验结果、判定结论等,同时要注明检测方法和参考范围等相关信息。
4 结语
分子诊断试剂设计开发时要严格按照生产质量管理体系,保证各环节有序开展,尤其是注册体系核查时要按照标准执行,确定医疗器械生 范要求 品质量以及产品研制、设计开发等内容贯彻落实到实处。分子诊断试剂设计被看作是产 质量控制的要点,同时也是生产质量控制的主要依据,所以要结合产品技术原理,确保整个设计开发过程的完整性、系统性,为产品安全质量提供保证。
[1] 陈久凯 , 谢在春 , 张战锋 , 等 . 临床分子诊断检验技术教学带教经验思考与实践 [J]. 实用检验医师杂志 ,2024,16(04):376-380.
[2] 尹佳祺 , 折小娟 , 和林洁 , 等 . 基于 CRISPR/Cas 的分子诊断技术在病毒检测中的应用 [J]. 检验医学与临床 ,2024,21(20):3100-3104.
[3] 刘秉春 , 袁建龙 . 基于诊断试剂研发的产学研结合教学改革在临床检验诊断学见习中的探索 [J]. 内蒙古医科大学学报 ,2022,44(S1):1-2+5.
[4] 方枫玲 , 郭绍彬 , 傅亚 , 等 . 基于立足开关的无细胞转录翻译系统及其在感染性疾病分子诊断中的应用 [J]. 福建医科大学学报 ,2022,56(03):277-280.
[5] 蔡贞 , 李书芬 , 籍会彩 , 等 . 医学检验专业分子诊断实习带教方法探讨 [J]. 分子诊断与治疗杂志 ,2022,14(05):899-902.
作者简介:李弘韬(1986.10-),男,汉族,湖南常德,硕士研究生,中级职称,主要从事分子检验、试剂研发相关工作
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)