艾司奥美拉唑方案治疗慢性胃炎患者反流的疗效

徐培容
上海市青浦区重固镇社区卫生服务中心 上海 201706
慢性胃炎是消化系统常见病,全球发病率随年龄增长呈上升趋势,我国流行病学调查显示其患病率约为 50%[1] 。反流症状(如烧心、反酸)在慢性胃炎患者中发生率高达 40%~60% ,不仅影响生活质量,还可能加速胃黏膜萎缩、肠化生等病理进程[2]。胃食管反流与胃酸分泌异常、食管下括约肌功能障碍及胃动力异常密切相关,而胃酸过度分泌是导致胃黏膜损伤的核心机制之一。艾司奥美拉唑作为新一代质子泵抑制剂(PPI),是奥美拉唑的S-异构体,通过特异性抑制胃壁细胞 H+/K+ -ATP 酶活性,阻断胃酸分泌的终末环节,其抑酸作用强、起效快且持续时间长[3]。既往研究表明,PPI 类药物在反流性食管炎治疗中疗效显著,本研究通过前瞻性随机对照试验,探讨艾司奥美拉唑单药方案对慢性胃炎患者反流症状,为临床优化治疗方案提供依据。
1 资料与方法
1.1 一般资料
选取我院 2023 年 9 月至 2024 年 9 月门诊治疗的 100 例慢性胃炎伴反流症状患者作为研究对象,采用随机数字表法将100 例患者分为观察组(50例)与对照组(50 例)。纳入标准: ① 符合《慢性胃炎中西医结合诊疗共识意见(2017 年)》中慢性胃炎诊断标准,经胃镜检查证实胃黏膜存在慢性炎症(充血、水肿、糜烂等); ② 近4 周内至少每周出现2 次烧心或反流症状; ③ 年龄 18~65 岁,性别不限; ④ 患者签署知情同意书。排除标准:① 合并消化性溃疡、胃癌、食管癌等严重器质性疾病; ② 近 1 个月内使用过 PPI、H2 受体拮抗剂或促胃肠动力药物; ③ 严重肝肾功能不全、妊娠或哺乳期女性; ④ 对艾司奥美拉唑过敏者。两组患者基线资料(性别、年龄、病程、症状评分)比较,差异无统计学意义( P>0.05 ),具有可比性。
1.2 方法
观察组给予艾司奥美拉唑肠溶 20mg ,每日早餐前30 分钟口服,连续用药 8 周;对照组给予外观、剂型与艾司奥美拉唑相同的安慰剂(主要成分为淀粉),用法用量与观察组一致。两组患者均接受相同的生活方式指导(如避免暴饮暴食、睡前2 小时禁食等),治疗期间禁止使用其他抗酸药物或促胃肠动力药物。
1.3 观察指标
1.3.1 症状评分:采用视觉模拟评分法(VAS)评估烧心、反流症状严重程度(0 分 ⋅= 无症状,10 分 Ψ=Ψ 无法忍受),同时记录每周烧心、反流发作频率(次数/周)。1.3.2 血清炎症因子检测:治疗前后采集空腹静脉血 5mL ,离心分离血清后,采用酶联免疫吸附试验(ELISA)检测C 反应蛋白(CRP)、降钙素原(PCT)。
1.4 统计学方法
采用SPSS 26.0 软件进行数据分析。计量资料以均数  标准差(
标准差( 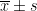 )表示,组间比较采用独立样本 t 检验,组内治疗前后比较采用配对样本 t检验;计数资料以例数 (% )表示,组间比较采用 χ2 检验。以 P<0.05 为差异有统计学意义。
)表示,组间比较采用独立样本 t 检验,组内治疗前后比较采用配对样本 t检验;计数资料以例数 (% )表示,组间比较采用 χ2 检验。以 P<0.05 为差异有统计学意义。
2 结果
2.1 对比分析两组治疗前后症状评分,观察组烧心评分、反流评分及发作频率均显著低于对照组( P<0.05 ),且观察组治疗前后差值均大于对照组(表1)。
表1 两组治疗前后症状评分比较( 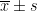 )
)

2.2 对比分析两组血清炎症因子水平变化,两组C 反应蛋白(CRP)、降钙素原(PCT)均较治疗前显著下降( P<0.05 ),且观察组下降幅度更显著( P<0.05 ,表2)。
表2 两组血清炎症因子水平比较(x ± s )

3 讨论
艾司奥美拉唑治疗慢性胃炎伴反流的疗效与机制密切相关,其通过抑制胃壁细胞 H+/K+-ATP 酶阻断胃酸分泌终末环节,显著降低反流症状评分及24 小时酸暴露时间,同时可改善胃黏膜炎症分级,形成“抑酸-抗炎-修复”效应[4]。单药方案安全性良好,不良反应发生率低,为临床提供了无需联合用药的高效选择,尤其适用于轻中度症状患者的精准治疗。
参考文献
[1]徐成龙,程海俐,张彩凤,等.艾司奥美拉唑方案治疗慢性胃炎患者反流的临床研究[J].临床消化病杂志,2024,36(4):265-269.
[2]陈晖,蔡红,黄胤,等.康复新液治疗反流性食管炎合并 Hp 感染慢性胃 炎的临床分析[J].海峡药学,2022,34(7):98-100.
[3]王玉晓,梁昊,王新宙,等.米曲菌胰酶与伊托必利联合治疗慢性胃炎伴反流性食管炎患者的效果分析[J].中国伤残医学,2024,32(21):67-70.
[4]雷琳.奥美拉唑治疗慢性胃炎伴反流性食管炎对患者焦虑、抑郁评分以及治疗总有效率的影响探讨[J].饮食保健,2021(31):103-104.
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)