大肠杆菌对高浓度丙二酸盐耐受性研究

刘晓瑜
青岛农业大学
引言
目前,研究人员主要通过增强Malonyl-CoA 供给,减少Malonyl-CoA 消耗以及精细调控Malonyl-CoA 水平等代谢工程策略来提升菌株生产Malonyl-CoA 下游衍生物的能力。然而,大肠杆菌等模式生物中主要的Malonyl-CoA 合成路径是乙酰辅酶A 羧化酶(ACC)催化乙酰辅酶 A 生成Malonyl-CoA,且胞内 ACC 合成受到严格和复杂的调控。因此,Malonyl-CoA 的供给能力仍然不足,这成为下游衍生物高效合成的重要限制因素之一。本文对已构建的菌株进行针对丙二酸的适应性实验室进化以进一步促进菌株对Malonyl-CoA 的供给能力。
1.研究基础
1.1 菌株和质粒
本文所用菌株及质粒如下表所示:
表 1 - 1 菌株和质粒
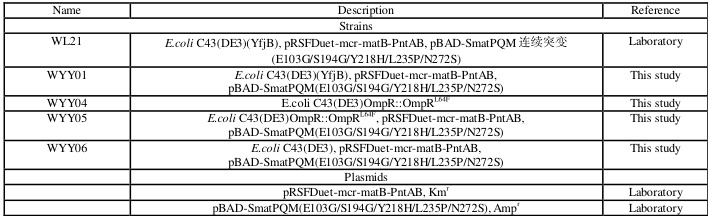
1.2 引物序列
表 1 - 2 本实验所用引物
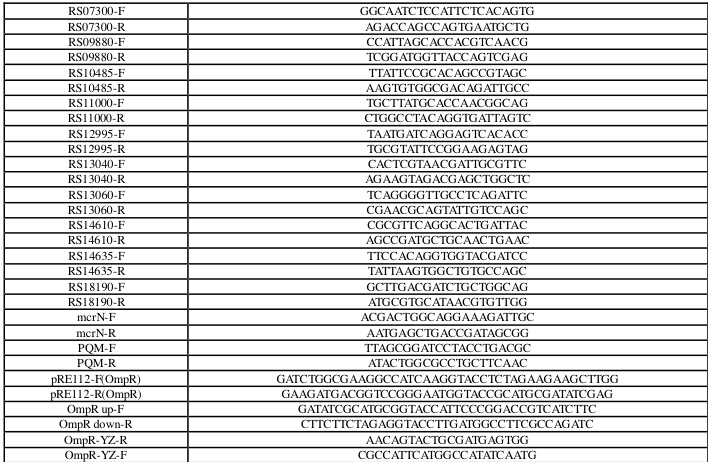
2.研究方法
2.1 菌株 WL-6 适应性实验室进化
1)将菌株WL-6 从保菌管中接至 10 mL LB 培养基(加入氨苄青霉素和卡那霉素抗性)中活化,按1%的接种量转接至10 mL M9 培养基,37 ℃活化 24 h,连续活化两代,设为实验组;另将菌株WL-6 从保菌管中划线到 LB 平板上,挑单菌接种到M9 液体培养基中,作为对照组。
接菌。按照3 %的接种量将过夜活化的菌株接种到50 mL M9培养基中加入相应浓度的3M丙二酸钠一水合物(初始耐受浓度为30 mM),于 37 ℃摇床培养。
2)生长曲线测定。测定加入诱导物后0 h、3 h、5 h、8 h 的 OD600 值。当实验组菌株的生长受到较为明显的抑制时,将菌株在加有相应浓度丙二酸盐的M9 平板上进行划线,挑取单菌落进行活化,并对所选菌株进行 16S 测序,确定菌株无污染后对活化菌株进行下一步进化。
3)质粒验证。对菌株内的基因mcr 及质粒Pbad-SmatPQM 进行扩增,验证验证质粒是否存在
2.2 HPLC 测定丙二酸盐转运及 3-HP产量
对-20 ℃保存到菌液上清进行HPLC 测定。将活化菌株转接至50 mL 发酵培养基中,37℃摇床培养至OD600 Σ=Σ 0.6~0.8,加入诱导剂100 mg/mL L-阿拉伯糖 500 μL, ,1 MIPTG 30 μL,30 ℃诱导表达 16 h,取 1 mL 菌液,12000 rpm,离心 5 min,取上清进行 HPLC 测定。2.3 菌株基因组 OmpRL64F 突变及测定
1)接菌双交换菌株及 C43(DE3)单菌接至10 mL 的 LB 液体培养基中,37 ℃活化,转接 10 mL 的 M9 液体培养基中,37 ℃摇床培养,连续转接两代;
2)按照 1%的接种量转接至 50 mL M9 液体培养基中,测定菌株生长曲线。
3)接菌株 ZXP34 至 10 mL 的 LB 液体培养基中,用于提取质粒 pRSF-mcr-matB-pntAB;
4)将双交换菌株及C43(DE3)转接至10 mL 的 LB 液体培养基中,37 ℃摇床培养,用于制备感受态;
5)制备双交换菌株及 C43(DE3)感受态,共转化质粒 pBAD-SmatPQM 连续 5 个突变及质粒 pRSF-mcr-matB-pntAB;
6)接菌。将双交换菌株20 及 C43(DE3)单菌的转化子接至 10 mL 的 LB 液体培养基中,37 ℃活化,转接 10 mL 的 M9 液体培养基中,37 ℃摇床培养,连续转接两代;
7)按照 1%的接种量转接至 50 mL M9 液体培养基中,测定菌株生长曲线。
3.研究结果
3.1 菌株丙二酸盐耐受度结果
当丙二酸盐浓度为 57.3 mM 时,实验组菌株生长未出现抑制现象,可继续增加丙二酸盐浓度对实验组菌株进行丙二酸盐耐受。当丙二酸盐浓度为 205.3 mM 时,实验组菌株的生长收到较为明显的抑制。当丙二酸盐浓度为 246.3 mM 时,对菌株1-1 进行连续三天的同一浓度耐受,数据显示,菌株1-1 的生长有较为明显的改善,故将提高丙二酸盐的浓度对菌株 1-1 进行耐受培养。提高 10 %的丙二酸盐耐受浓度,对菌株1-1 进行培养。
当丙二酸盐浓度为 270.9 mM,菌株在此浓度下生长过于缓慢,对菌株1-1 进行连续转接以达到耐受目
当丙二酸盐浓度为 313.8 mM 时,菌株 1-1 的生长状况同丙二酸盐浓度为 298.8 mM 时的大致相同,继续以5 %的增量提高丙二酸盐浓度对菌株1-1 进行耐受。
当丙二酸盐浓度为 363.6 mM 时,菌株 1-1 的生长趋势无明显差异,继续提高5 %丙二酸盐浓度对菌株1-1 进行耐受丙二酸盐浓度为 381.9 mM 时,菌株 1-1 经连续五代转接耐受后,生长状况达到前一丙二酸浓度时的生长水平当丙二酸盐的耐受浓度达到400mM,菌株 1-1 生长稳定。
3.2 HPLC 测定结果
丙二酸盐的转运效率从3.1%提高至 11.18%,转运量增加了 48.23 倍。3.3 重测序突变筛选结果
3.3.1 重测序结果
表 1 - 3 重测序结果
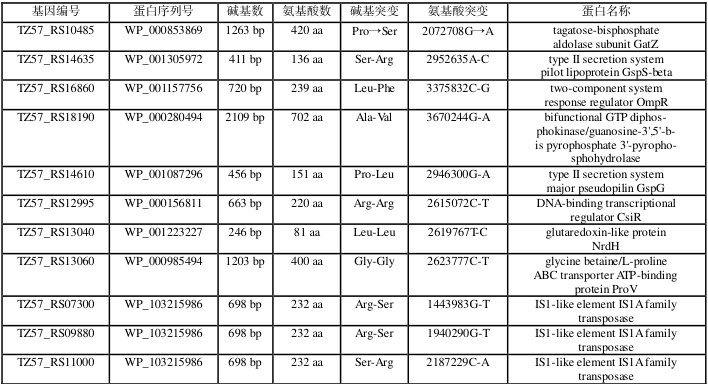
表 1 - 4 重测序鉴定结果
3.3.2 E.coliC43 基因组 OmpRL64F突变
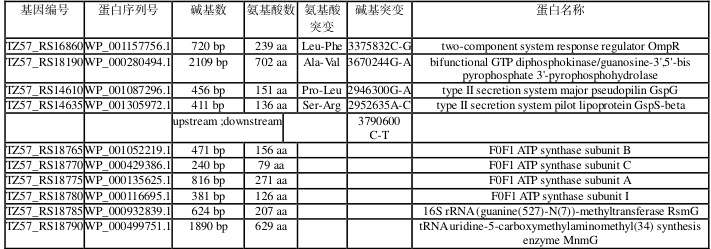
图 1 - 1 未共转质粒菌株生长测定
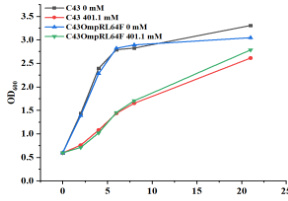
图 1 - 2 共转质粒菌株生长测定
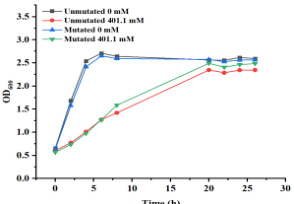
研究表明:在401.1mM 高浓度丙二酸盐的条件下,突变菌株适应性较强,表明E.coli C43 基因组 0mpR∣β+∣ 位点突变对菌株的丙二酸盐耐受有正向作用。
参考文献:
[1] Nam, K.K., et al, Engineered methane biocatalysis: strategies to assimilate methane for chemical production. Chem Biotechnol, 2024.85:1-8.
[2] Kaku, M., et al., Fatty Acid Production by Enhanced Malonyl-CoA Supply in Escherichia coli. Curr Microbiol, 2022. 79(9): p. 269.
[3] Liang, B., et al., Production of 3-hydroxypropionate using a novel malonyl-CoA-mediated biosynthetic pathway in genetically engineered E. colistrain. Green Chem, 2019. 21(22):6103- 6115.
[4] Liang, B., et al., Directed evolution of tripartite ATP-independent periplasmic transporter for 3-Hydroxypropionate biosynthesis. Appl Microbiol Biot, 2023. 107:663-676.
[5]Wu, Y.N., et al., Advanced strategies and tools to facilitate and streamline microbial adaptive laboratory evolution. Trends Biotechnol, 2022. 40(1):38-59.
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)