红外线疗法对CUMA大鼠抑郁样行为的干预及海马谷氨酸转运体的调节作用

张敬梓 王佳怡
山东第一医科大学(山东省医学科学院)运动医学与康复学院 泰安 山东 271000
抑郁症是全球范围内常见且严重的精神疾病,是全球致残的主要原因[1]。抑郁症的机制研究大多聚焦于单胺递质假说[2],但其并不能完全解释抑郁症的发病机制,开发新的治疗策略并寻找有效的分子作用靶标对抑郁症治疗至关重要。研究表明红外线疗法能够改善老年小鼠和阿尔茨海默症小鼠的认知能力及相关的病理变化[3],但其在改善机体抑郁症状中的相关研究尚较少,且神经递质谷氨酸在其中的作用机制尚不明确。本研究通过制备慢性不可预知应激 (chronic-unpredictable mild stress, CUMS)大鼠模型,在观察抑郁样行为及海马谷氨酸转运体变化的基础上进一步给予红外线疗法干预,探讨红外线疗法对抑郁大鼠行为的干预作用及机制,对临床抑郁症的改善及防治具有重要意义。
一、研究方法
以雄性 SD 大鼠 40 只为研究对象,随机选取 10 只为正常大鼠对照组,10 只为正常大鼠干预组,其余制备 CUMA 大鼠模型后随机分为 CUMS 大鼠对照组和干预组,每组 10 只。对照组给予正常饮食,不进行红外线照射;干预组给予正常饮食,加以红外线疗法干预,30min/次,2 次/日,15 天/疗程,间隔 3 天进行下一个疗程。每周记录大鼠体重;评价大鼠抑郁样行为;取海马组织,免疫印迹法检测谷氨酸转运体-2 的蛋白表达。
采用 SPSS20.0、Graphpadprism 软件进行数据统计分析以及图像化处理,用单因素方差分析各组间数据,以 p<0.05 表示有统计学意义, p<0.01 表示有显著性差异。
二、研究结果
1.各组实验动物体重的比较结果
造模前各组大鼠体重差异不大 (p>0.05) ),CUMS 大鼠体重呈现下降的趋势,差异具有统计学意义 (p<0.05) )。经过 4 周红外线照射干预后,与正常组大鼠相比,干预组大鼠体重明显上升 (p<0.05) )。 表明红外线可以有效提高 CUMS 大鼠的体重,改善小鼠抑郁现象。见图 1。
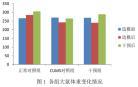
2.各组蔗糖偏好测定结果
与正常大鼠相比,CUMS 组大鼠蔗糖偏好指数显著降低 (p<0.01) ),经过 4 周红外线照射后,与 CUMS 正常组相比,干预组大鼠的蔗糖水偏好百分数显著增加,差异具有统计学意义( p<0.01) )。见图 2。

3.强迫游泳实验结果
与正常大鼠相比,CUMS 组大鼠强迫游泳不动时间显著增加,差异具有统计学意义 (p<0.01) ),红外线照射后,干预组大鼠的强迫游泳不动时间较 CUMS 对照组显著降低 (ρp<0.05) )。见图 3。

4.谷氨酸转运体-1 的表达
与正常对照组(2.45±0.27)相比,CUMS 对照组大鼠海马的谷氨酸转运体-2 的蛋白表达(1.87±0.32)显著减少( (p<0.05) )。与CUMS 对照组相比,干预组大鼠海马谷氨酸转运体-2 的蛋白表达(2.03±0.26)显著增加( (p<0.05) )。
三、讨论
红光到红外光治疗,特别是近红外范围内的光,正在成为一种能够阻止神经元病变的安全有效的治疗方法[4]。CUMS 抑郁模型大鼠是由多种随机刺激诱导产生,这些随机刺激与人类生活中的应激事件相似。本研究中,经过 4 周慢性不可预知刺激后,我们发现 CUMS 大鼠体重显著下降,干预组大鼠体重明显上升,表明红外线照射可以有效提高 CUMS 大鼠的体重,改善大鼠抑郁现象。
采用蔗糖偏好实验、强迫游泳实验检测模型动物的抑郁样行为。本研究发现 CUMS 刺激构建抑郁造模后,大鼠对蔗糖的偏好性降低,提示抑郁大鼠较 大鼠出现快感缺失的现象;强迫游泳不动时间明显增多,提示抑郁大鼠较正常大鼠求生欲降低。红外线照 CUMS 大鼠对蔗糖的偏好性,减少强迫游泳不动时间,表明红外线照射可以提高 CUMS 抑郁大鼠的喜好及求生欲,改善大鼠抑郁样行为。
谷氨酸能系统在重度抑郁症的病理和治疗中起着重要作用[5]。本研究对蛋白检测的结果表明,抑郁症大鼠海马谷氨酸转运体-2 的表达显著降低;在给予红外线疗法干预后, 干预组大鼠海马谷氨酸转运体-2 的蛋白表达明显升高。本研究认为,红外线治疗可有效调控谷氨酸能系统的功能,其可能是通过调控谷氨酸转运体-2 的表达进而发挥治疗作用。
四、结论
抑郁大鼠体重减轻、糖水偏好减少、强迫游泳不动时间延长,且海马谷氨酸转运体-2 蛋白表达显著减少,而红外线照射可以通过调节谷氨酸转运体的表达有效改善CUMS 抑郁大鼠的症状。
参考文献:
[1] Malhi GS, Mann JJ. Depression. Lancet. 2018;392(10161):2299-2312.
[2] Chen Y, Cai W, Li C, et al. Sex differences in peripheral monoamine transmitter and related hormone levels in chronic stress mice with a depression-like phenotype. PeerJ. 2022;10:e14014.
[3] Du B, Zou Q, Wang X, et al. Multi-targeted engineered hybrid exosomes as Aβ nanoscavengers and inflammatory modulators for multi-pathwa ntion in Alzheimer's disease. Biomaterials. 2025;322:123403.
[4] Johnstone DM, Moro C, Stone J, Benabid AL, Mitrofanis J. Turning On Lights to Stop Neurodegeneration: The Potential of Near Infrared Light Therapy in Alzheimer's and Parkinson's Disease. Front Neurosci. 2016;9:500.
[5] Tokita K, Yamaji T, Hashimoto K. Roles of glutamate signaling in preclinical and/or mechanistic models of depression. Pharmacol Biochem Behav. 2012;100(4):688-704.
第一医科大学校级大学生创新创业训练计划项目2024104390372
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)