疫苗运输用冷链车验证URS的编写要点

陈刚 石璐 任海 李兴安 岳兰瑜
兰州生物制品研究所有限责任公司 甘肃兰州 730046
中图分类号 :F426.72 文献标志码 :A
1、概述
疫苗作为特殊的生物制品,其质量和有效性高度依赖于从生产到接种全过程的冷链运输环节。冷链车作为疫苗运输的关键载体,其性能直接影响疫苗质量安全。质量源于设计,一个良好的 URS 是进行后续验证工作的基础[1]。编写疫苗运输用冷链车验证 URS(用户需求说明)时,需紧密围绕法规要求、行业标准及实际应用需求,确保冷链车满足疫苗运输的严苛条件,实现产运销全链路品质提升[2]。
从法规要求来看,国内外均有严格的规定保障疫苗运输安全。在中国,《中华人民共和国疫苗管理法》明确指出疫苗储存、运输应当符合疫苗储存、运输管理规范,保证疫苗质量。《药品经营质量管理规范》(GSP)对冷链药品运输设备的温度控制、监测、记录等提出详细要求,冷链车需具备自动调控温度、自动监测、数据存储及可追溯等功能。在编写URS 时,必须将这些法规条款细化为具体的技术要求,如冷链车温度传感器的精度需达到 ±0.5‰ ,温度数据的存储时间不得少于 5 年等,确保法规要求得到切实落实。企业可以通过贯穿于产品生命周期全过程的确认或验证工作来证明影响质量的关键要素能够得到有效控制,为持续生产出合格产品提供保证[3]。
行业要求也是编写 URS 的重要依据。医药冷链物流行业经过多年发展,形成了一系列成熟的标准和规范。中国医药商业协会发布的《药品冷链物流运作规范》,对冷链车的制冷系统、保温性能、温度监测设备等进行了规范。例如,要求冷链车在外界环境温度 - 30℃至 40℃范围内,能够将厢内温度控制在规定的疫苗储存温度区间,且温度波动范围不得超过 ±2C 此外,行业内普遍要求冷链车配备双制冷机组或备用电源等应急保障设施,以应对突发情况,保障疫苗运输安全。同时,随着技术发展,行业对冷链车的智能化水平要求也日益提高,如实时远程温度监控、异常报警等功能成为标配。URS 需明确这些行业技术指标和功能要求,确保冷链车符合行业先进水平。
除法规和行业要求外,疫苗运输的实际应用场景需求也不容忽视。不同类型的疫苗对温度的敏感度不同。因此,URS 应根据疫苗的具体特性,对冷链车的温控范围、温度均匀性等提出针对性要求。同时,考虑到长途运输、频繁装卸货等实际情况,需对冷链车的制冷效率、保温性能衰减情况等进行详细规定[4]。在验证方面,需明确空载验证、满载验证、极端环境验证等不同场景下的验证方法和合格标准,确保冷链车在各种工况下均能稳定运行。此外,数据管理也是关键环节,URS 应规定温度数据的采集频率、传输方式、存储格式等,保证数据的真实性、完整性和可追溯性。
综上所述,疫苗运输用冷链车验证 URS 的编写需全面考量法规要求、行业标准和实际应用需求,将宏观的政策规范转化为可操作、可验证的具体技术指标和功能要求,从而为疫苗运输安全提供坚实保障。
2、冷链车验证URS 编写框架
疫苗冷链运输车的主要作用为保障疫苗运输环节的温度控制在 2-8℃范围内。用户需求文件总括了用户对疫苗冷链运输车的质量要求,也描述了用户对疫苗冷链运输车的工作过程及功能期望。要点如下:
下文针对A 生物制药公司冷链车URS 作为实例进行讨论。
3、冷链车验证 URS 的编写要点
3.1 仪器性能及技术参数要求

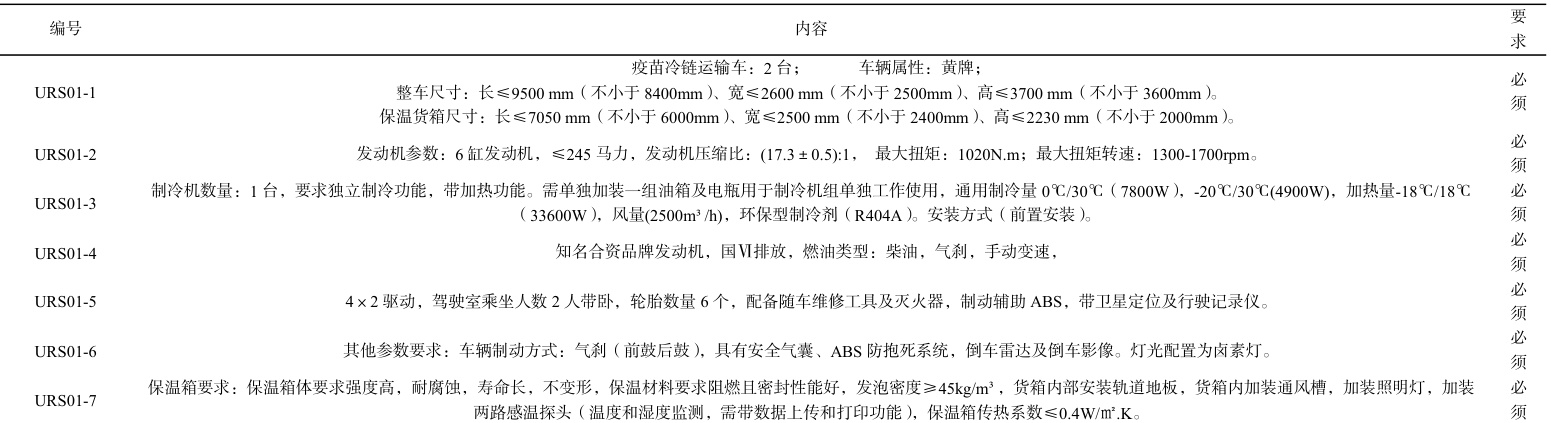
3.2 控制系统要求

3.3 备品备件及仪表要求


3.4 外观及材质要求
箱体内外平整光滑,内部无死角。箱体内外表面耐酸耐碱耐燃。箱体内表面应能耐受消毒剂如甲醛、乙醇、臭氧、过氧化氢等的腐蚀。
3.5 安全要求
设有必要的保护设施或措施,保证在设备出现故障或控制失效时设备、人员均处于安全状态。设备应能有效接地,并能有效防止静电产生。车厢门锁需为双锁。
3.6 设施/公用系统要求
制冷系统及车辆电子元件均需达到国家标准。
3.7 电力要求
交流 220V、单相三线制,50Hz。所有的线路应尽量在内部。所有电缆终端应卷曲包好线头做好相应标记。
3.8 清洁要求
表面光洁易于清洁,物料接触处无死角。
3.9 文件要求
供应商须提供文件清单、产品合格证、质量证明书。须提供纸版和电子版设备使用维护说明书。须提供设备出厂前的安装、运行及性能确认文件。须提供中文的纸版和电子版设备操作、清洗和维护检修规程、验证文件、温/湿度控制文件。
3.10 安装调试要求

用户应与供应商签订该设备的合同、图纸设计、交货期、厂家验收测试、发运时间、调试、现场验收测试及后续确认工作的进度要求。
3.11 验证或计量要求
供应商应提供设备用仪器仪表校验报告、计量证书。应提供详细的符合相关规范、车厢的验证文件(IQ、OQ、PQ、计算机化系统验证(温度控制系统),提供电子版供审查,完成验证方案及验证工作。IQ、OQ、PQ 验证所需材料及设备,由供应商负责提供。各类验证测试仪器,应提交有CNAS资质的计量证书。依据设备设计功能说明、设计技术指标及约定内容逐项验收。
3.12 培训
交货前,供应商负责免费对用户的技术人员、操作人员、维修人员进行以设备结构原理、性能、操作、维修、常见故障排除等基本知识为内容的工厂培训和考核,培训人员不少于3 人,保证操作人员能够独立操作设备,维修人员能对常见故障进行处理。现场调试期间,供应商负责免费对用户现场的操作和维修人员进行培训,保证操作人员能够独立操作设备,维修人员能对常见故障进行处理。
3.14 包装及运输
运输过程中防磕碰、防振动,由于包装不良而造成的任何损坏,供应商承担全部损失和费用。运输时间包含在供货周期内,供应商负责运输,承担运输费用。该设备必须有到货清单,详细列内容物。到货时供应商必须陪同现场人员进行验收,若供应商授权用户自行验收,如发现机器及零配件有任何损坏、缺少,供应商应负全责。供应商负责将需方订购设备送至用户单位。供应商必须指派技术人员进行现场指导。供应商负责设备运送至需方厂内、安装、调试等设备移交验收前的各项费用。
3.13 进度要求

3.15 质量保证
设备的设计、制造、材质符合使用方要求。满足现行国家、行业规范及有关规定。
3.16 售后服务
3.17 变更管理
在设备设计、制造、运输、交付、安装、调试、验证过程中发生的任何变更均应按照用户的变更控制流程进行,经QA 批准后,及时修订相关文件。
4、结语
疫苗作为特殊生物制品,其质量与有效性高度依赖冷链运输,冷链车性能至关重要,而良好的 URS是后续验证工作的基础。编写疫苗运输用冷链车验证 URS 需结合法规、行业标准及实际需求,确保冷链车符合温控等质量安全规范。文中给出冷链车验证 URS 编写框架,涵盖仪器性能、控制系统等 17个项目。以 A 生物制药公司为例,从技术参数、控制功能、安全要求等方面详述编写要点,涉及温度控制、数据记录、应急保障等关键指标,还对安装调试、验证流程、培训及售后等环节提出具体要求,为保障疫苗运输安全提供了可操作的技术规范。
参考文献:
[1]杨睿雅,梁毅.GMP 中间体生产厂房验证 URS 的编写要点[J].化工设计通讯,2021,47(08):189-191.
[2]杨晓晶.乳品冷链从保障链转向价值链[N].中国食品报,2025-05-06(004).
[3]陈炜,申琦,梁毅.基于风险管理的 GMP 验证在医疗器械生产企业中的应用[J].沈阳药科大学学报,2024,41(11):1519-1530.DOI:10.14066/j.cnki.cn21-1349/r.2022.1048.
[4]Shi, Huaixia,Zhang, Qinglei,Qin, Jiyun.Cold Chain Logistics and Joint Distribution: A Review of Fresh Logistics Modes[Z].SYSTEMS,2024,12(7).
作者简介 :陈刚(1995—),男,硕士,主要研究方向为药事管理,药品质量认证(GMP GSP GLP)。
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)