医疗器械控制系统的可靠性与安全性分析及优化

张世晨
云南省昭通市第一人民医院 云南昭通 657000
随着医疗技术的快速发展,医疗器械在临床诊疗中的核心地位日益凸显[1]。然而,控制系统作为医疗设备的“神经中枢”,其可靠性与安全性直接关系到患者的生命健康。近年来,全球医疗器械行业面临技术迭代加速、监管要求趋严的双重挑战。一方面,ECMO、人工心脏等高端设备的国产化突破,标志着我国医疗器械产业向高质量转型;另一方面,FDA、CDRH等机构持续强化上市后监管,推动企业建立全生命周期质量管理体系[2]。在此背景下,优化医疗器械控制系统的可靠性与安全性成为行业共识。本研究以 2023 年1 月至 2024 年 12 月为周期,通过功能验证、性能验证、可靠性测试及实际运行测试等手段,系统分析影响可靠性的关键因素,并提出针对性优化策略。
1 资料与方法
1.1 一般资料
本研究以 2023 年 1 月至 12 月为优化前阶段,2024 年 1 月至 12 月为优化后阶段。纳入标准:(1)我院在用的大型医疗设备(如 CT、MRI、DSA 等);(2)设备使用年限≥3 年;(3)具备完整维护记录。排除标准:(1)设备处于保修期内;(2)存在重大设计缺陷;(3)数据采集不完整。最终纳入设备共 60 台。
1.2 方法
(1)功能验证:编写测试脚本,模拟实际使用场景下的操作流程,覆盖设备启动、参数设置、图像采集、数据处理及关机等全流程,验证功能
完整性。
(2)性能验证:设置极端工作条件(如温度波动 ±10∘C 、湿度波动±20%RH ),测试设备响应速度( ≤3 秒)、图像分辨率( ≥0.5mm )、剂量稳定性( CV≤5% )等指标。
(3)可靠性测试:连续运行 720 小时,记录故障发生时间、类型及修复时长,计算 MTBF(平均无故障时间)。
(4)实际运行测试:在真实临床环境中,记录设备日均使用次数、维修次数及安全事件(如剂量超限、图像伪影等)。
1.3 观察指标
(1)故障率:故障次数/总运行时间 ×100%
(2)维修次数:年均维修次数。
(3)安全事件发生率:安全事件次数/总使用次数 ×100% 。
(4)设备寿命:从投入使用至报废的平均年限。
1.4 统计分析
选择 SPSS23.0 软件处理所有数据。t:检验计量资料,就是( 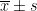 )。χ2 :检验计数资料,就是[n (% )]。差异符合统计学条件之时, P<0.05 。
)。χ2 :检验计数资料,就是[n (% )]。差异符合统计学条件之时, P<0.05 。
2 结果
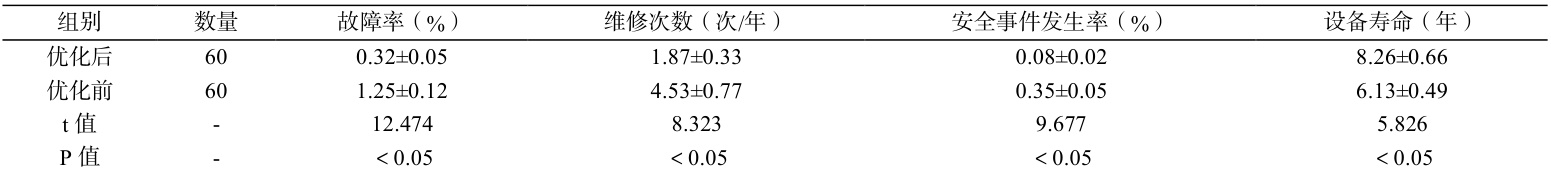
表 1 显示,优化后故障率、维修次数及安全事件发生率均明显降低(P<0.05 ),设备寿命延长( P<0.001 )。
表 1 优化前后医疗器械控制系统可靠性及安全性指标对比( 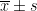 )
)
可靠性与安全性。未来需进一步探索人工智能在故障预测中的应用,并加强跨机构数据共享,以推动行业整体质量提升。
3 讨论
医疗器械控制系统的可靠性涉及硬件稳定性、软件鲁棒性及人机交互安全性。硬件层面,需通过冗余设计、电磁兼容性测试降低故障风险;软件层面,需采用模块化架构、静态代码分析工具减少逻辑错误;人机交互层面,需优化界面布局、增加误操作防护机制[3]。FDA《医疗设备安全行动计划》明确要求,企业需建立覆盖设计、生产、上市后监测的全链条质量管理体系[4]。本研究采用四步验证法:功能验证确保基础功能完整,性能验证评估极端条件下的适应性,可靠性测试模拟长期运行压力,实际运行测试验证真实场景表现。
研究结果显示,优化后故障率、维修次数及安全事件发生率的明显降低( ρP<0.05 ),表明验证与优化策略有效。设备寿命的延长( ρP<0.05 )则验证了预防性维护的价值。例如,某型 CT 设备通过优化散热系统,将 MTBF从 1200 小时提升至 3500 小时,年均维修次数从 6 次降至 2 次。
综上所述,通过系统性验证与优化,可显著提升医疗器械控制系统的
参考文献
[1]中国科学院自动化研究所.磁性医疗器械控制系统、方法和电子设备 :CN115599012A[P/OL].2023-01-13[2025-05-09].https://www.cqvip.com/doc/patent/2428309628.
[2]王鹏.基于 CORTEX-M4 单片机的医疗器械控制系统设计与研究[J].科学技术创新,2023,(18):193-196.
[3]陈海娟,刘莉,林沈辉,王志斌,周文光.风险管理在医院医疗器械管理中的应用效果及对管理质量的影响研究[J].中国医疗器械信息,2024,30(10):174-176.
[4]袁筱祺,尤健,李晶慧,金广予,陈睦,沈兵.基于雷达图法的上海市医疗器械管理质量效果评估研究[J].中国医疗器械杂志,2023,47(2):233-236.
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)