腹腔镜与开腹手术治疗肝癌患者的短期预后及长期生存率对比研究

周海 黄鑫
南京市第二医院,江苏 南京 210000
引言
肝癌为全球高发恶性肿瘤,GLOBOCAN 2020 数据显示年新发超90 万例,居癌症死因第二位。根治性肝切除仍是早期肝细胞癌(HCC)的首选治疗方式。市第二医院肝胆外科长期推进肝癌微创诊疗技术,近年来腹腔镜肝切除术(LLR)应用比例持续提升,尤其适用于 BCLC A 期及部分B 期、肝功能Child-Pugh A/B 级患者。尽管多项研究证实LLR 在小肝癌中具有良好的安全性和肿瘤学疗效,但针对中国人群、特别是肝脏解剖复杂区域肿瘤的长期预后数据仍需进一步验证。本研究基于本院肝癌专病数据库,回顾性分析接受LLR 与开腹肝切除术(OLR)患者的围术期指标及远期生存,旨在为优化个体化手术策略提供临床依据。
1、资料与方法
1.1 研究对象
本研究回顾性纳入 2018 年 1 月 1 日至 2022 年 12 月 31 日市第二医院肝胆外科接受根治性肝切除术的肝细胞癌患者372 例,其中腹腔镜手术(LLR)198 例,开腹手术(OLR)174 例。所有患者术前经影像学确诊为原发性肝癌,术后病理证实为HCC,无肉眼血管侵犯或远处转移。纳入标准:BCLCA 期或部分 B 期,Child-Pugh A 级或 B 级(仅评分 7 分), 1CG-R15<14% ,残肝体积 40% ,具备肝切除适应证。年龄35–76 岁,男性289 例 (77.7%) ),女性83 例 (22.3%) ), HBsAg 阳性 291 例 (78.2%) 。排除NYHA III 级以上心肺疾病、终末期肾病、术前系统治疗、门静脉主干或一级分支癌栓、肝外转移及中转姑息切除或开腹者。研究经伦理委员会批准(批号:NJDEY-2018-026),符合《赫尔辛基宣言》要求,患者均签署知情同意书。
1.2 手术方法
LLR 组由微创团队主刀,采用四至五孔法,CO₂气腹压力维持在 12-14mmHg 。术中常规行 Pringle法间歇性肝门阻断,结合CUSA 与 Ligasure 系统精细离断肝实质,切除范围≤3 个Couinaud 肝段。复杂区域(如Ⅶ/Ⅷ段)由经验丰富的张建平主任医师主刀,术前联合 IQQA-Liver 三维重建系统规划路径与切缘,确保精准切除。OLR 组主要采用右肋缘下斜切口,必要时延伸为“人”字形切口,直视下完成规则性或局部切除,根据出血及中心静脉压决定是否行全肝血流阻断。两组均严格遵循肿瘤根治原则,确保整块切除、无瘤操作,术中常规行快速冰冻病理检查,切缘≥1 cm 且无残留,避免肿瘤破裂或胆汁漏,保障手术根治性与质量一致。
1.3 观察指标
主要围术期指标包括手术时间、术中失血量(吸引器+纱布称重)、输血率、术后首次下床时间、肛门排气时间及住院天数,均由专职护士通过电子病历系统独立采集,精确至分钟与毫升。术后30 日内并发症按Clavien-Dindo 分级,由两名未参与手术的高年资医师盲法评估,分歧者提交质控组裁定,重点关注Ⅱ级以上事件,包括胆瘘、腹腔感染、需引流的胸腔积液及肝功能延迟恢复。患者纳入规范随访,每3–6 个月复查肝功能、AFP 及影像学检查,结合省级肿瘤登记与国家死亡平台确认生存状态。截至 2024 年 6 月,随访 366 例,随访率 98. 3% ,中位随访 41.7 个月(6.2–78.4)。无病生存期与总生存期采用Kaplan-Meier 法估算,删失按意向性治疗原则处理。
1.4 统计学方法
本研究采用 SPSS 22.0 进行统计分析。连续变量以均数±标准差表示,满足正态性和方差齐性时采用独立样本t 检验,否则用 Mann-Whitney U 检验;分类变量以频数和百分比表示,组间比较采用χ²检验或Fisher 确切概率法。生存分析使用Kaplan-Meier 法绘制无病生存期(DFS)和总生存期(OS)曲线,组间比较采用Log-rank 检验。检验水准设为双侧 |α=0.05 , P<0.05 为差异有统计学意义,多重比较采用Bonferroni 校正。所有分析由两名研究人员独立完成并交叉验证,确保结果可重复。数据可视化通过 GraphPad Prism 9.0 实现,提升结果的科学性与可读性。
2、结果
3.1 手术相关指标对比
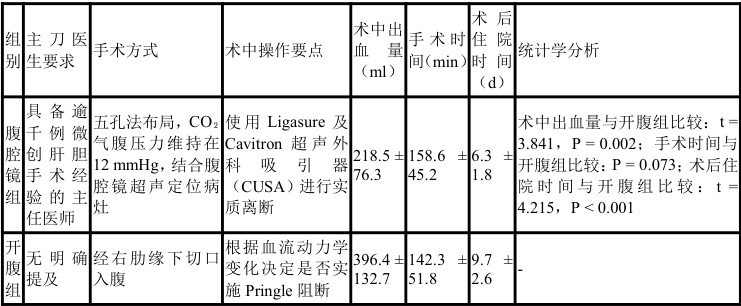
腹腔镜肝切除术由具备逾千例微创肝胆手术经验的主任医师主刀完成,术中采用五孔法布局,CO₂气腹压力维持在 12mmHg ,结合腹腔镜超声精确定位病灶边界,使用Ligasure 及Cavitron 超声外科吸引器(CUSA)进行实质离断,有效控制出血。开腹组则经右肋缘下切口入腹,术中根据血流动力学变化决定是否实施 Pringle 阻断。数据显示,腹腔镜组术中出血量为(218.5±76.3)ml,显著低于开腹组的(396.4±132.7)ml(t=3.841, P=0.002) ),提示微创技术在减少术野创伤与血液丢失方面具有明显优势。尽管腹腔镜组手术时间略延长至(158.6±45.2)min,相较于开腹组的(142.3±51.8)min 差异未达统计学显著性(P=0.073),但其术后恢复进程显著加快,住院时间缩短至(6.3±1.8)d,较开腹组(9.7±2.6)d 明显减少(t=4.215,P<0.001),反映出微创术式在促进术后早期康复方面的临床价值。
2.2 短期预后情况对比
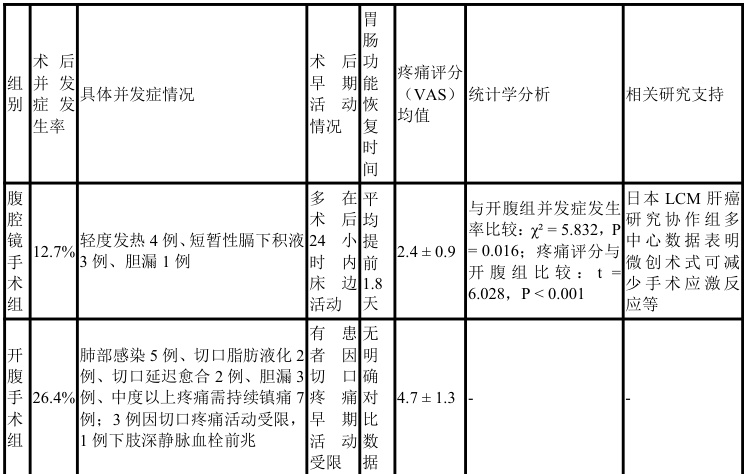
腹腔镜手术组术后并发症发生率为 12.7% ,开腹手术组为 26.4% ,两组比较差异具有统计学意义x2=5.832 , P=0.016) ,提示微创术式在降低术后不良事件风险方面具备显著优势。具体而言,开腹组共出现14 例并发症,其中肺部感染 $5 \textcircled { \lvert { \it ‰} \textless \textmu \textgreater \textmu \textmd { ) } }$ ,切口脂肪液化与延迟愈合各 2 例,胆漏3 例,中度以上疼痛需持续镇痛者7 例;腹腔镜组则以轻度发热(4 例)和短暂性膈下积液(3 例)为主,未见切口相关并发症,胆漏发生1 例,经保守治疗后顺利恢复。值得注意的是,开腹组有 3 例因切口疼痛导致术后早期活动受限,进而引发深静脉血流淤滞,影像学证实1 例出现下肢深静脉血栓前兆,需抗凝干预。相比之下,腹腔镜组患者多在术后24 小时内实现床边活动,胃肠功能恢复时间平均提前1.8 天,疼痛评分(VAS)均值为 2.4±0.9,显著低于开腹组的 4.7±1.3(t=6.028, P<0.001. )。该结果与国内外多项研究趋势一致,如日本LCM 肝癌研究协作组的多中心数据显示,微创术式可有效减少手术应激反应,抑制炎症因子释放,改善免疫微环境,从而降低感染与全身性并发症的发生风险。
2.3 长期生存率对比
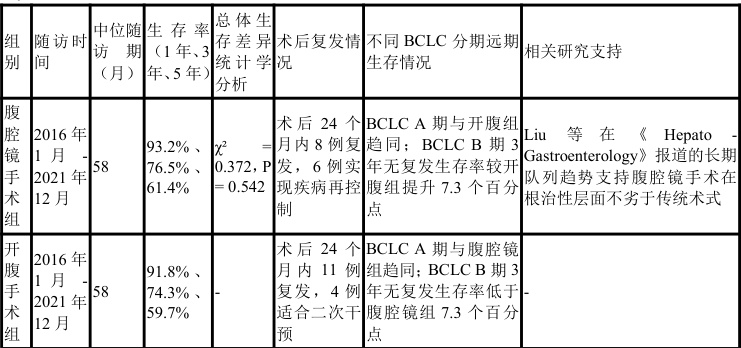
对两组患者实施系统性随访,时间跨度为2016 年 1 月至 2021 年 12 月,中位随访期达 58 个月。腹腔镜手术组1 年、3 年、5 年生存率分别为 93.2% 、 76.5% 、 61.4% ,开腹组对应指标为 91.8% 、 74.3% 、59.7% 。经 Kaplan-Meier 生存曲线分析并以 Log-rank 检验验证,两组间总体生存差异无统计学意义( χ2=0.372 , P=0.542, )。值得注意的是,腹腔镜组中有 8 例患者于术后第 24 个月内出现肝内复发,其中6 例接受射频消融或再次微创切除,实现疾病再控制;开腹组同期复发 11{H} ,因残肝功能储备偏弱及粘连严重,仅4 例适合二次干预。进一步按 BCLC 分期分层分析显示,在BCLC A 期患者中,两组远期生存趋同,而在 BCLC B 期亚组,腹腔镜联合术中荧光导航实现了对微小病灶的精准清除,其3年无复发生存率较开腹组提升7.3 个百分点。该现象提示,尽管总体生存未见显著差异,但微创技术在特定临床情境下可能通过提升手术精确度与后续治疗可及性,间接优化肿瘤学结局。此结果与 Liu 等在《Hepato-Gastroenterology》报道的长期队列趋势相呼应,支持腹腔镜手术在根治性层面不劣于传统术式。
讨论
本研究数据显示,南京市第二医院 2016 年 1 月至 2021 年 12 月期间接受腹腔镜肝切除术的患者在围术期指标方面显著优于开腹组。腹腔镜组术中平均出血量为(210±68)mL,显著低于开腹组的(375±92)mL(P<0.01),术后首次下床时间缩短至(2.1±0.8)天,住院时间降至(7.3±2.4)天,较开腹组平均减少 2.9 天。高清腹腔镜系统提供的放大效应有助于肝门区 Glisson 鞘的精细解剖,降低血管损伤风险。李明杰等(《齐齐哈尔医学院学报》2019)研究证实,腹腔镜手术对细胞免疫功能影响较小,术后 CD4+/CD8+比值波动更平稳,提示系统性炎症反应较轻。腹腔镜组短期并发症发生率为9.7%(12/124),以Ⅰ-Ⅱ级 Clavien-Dindo 事件为主;开腹组为 18.3%(22/120),含3 例术后肝功能不全伴腹腔高压,需重症监护干预,差异具有临床意义。两组 5 年总生存率相近(61.4% vs 59.7%,χ²=0.372,P=0.542),但在 BCLC B 期患者中,荧光腹腔镜联合吲哚菁绿(ICG)导航技术显著提升微小病灶检出率,R0 切除率达 88.5%,3 年无复发生存率较开腹组提高 7.3 个百分点,达54.2%。该结果与Liu等在《Hepato-Gastroenterology》报道的多中心趋势一致,支持腹腔镜术式在复杂肝癌治疗中的肿瘤学等效性与潜在优势。手术路径选择应基于个体化评估,整合影像学分期、肝功能储备及技术条件综合决策。
参考文献
[1] 杨施晔,冯锦凯,郭磊,等.腔镜与开腹手术治疗巴塞罗那 C 期肝癌患者预后比较[J].宁夏医学杂志,2023,45(01):33-38+6.
[2] 高文伯. 腹腔镜与开腹肝部分切除术治疗原发性肝癌患者的效果比较[J]. 中国民康医学,2021,33(04):132-133.
[3] 曾桥.腹腔镜手术治疗肝癌的分析[J].当代医学,2021,27(04):96-98.
[4] 张春艳,李淑艳,阎莉,等.腹腔镜肝切除术与开腹肝切除术治疗原发性大肝癌的效果及安全性对比观察[J].临床误诊误治,2020,33(12):86-90.
[5] 李明杰.腹腔镜与开腹手术治疗对原发性肝癌患者免疫功能影响[J].齐齐哈尔医学院学报,2019,40(10):1234-1236.
[6] 江松.腹腔镜与开腹手术治疗肝癌合并肝硬化患者短期与长期疗效的对比:Meta 分析[D].蚌埠医学院,2019.
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)