平均载体拷贝数方法优化及应用

高璇
上海泰昶生物技术有限公司 200131
1 概述
平均载体拷贝数(Vector Copy Number,VCN)是嵌合抗元受体T 细胞(CART)产品的重要安全性指标之一,是指通过病毒载体在 T 细胞的基因组中被整合的 CAR 拷贝数平均值。中国食品药品检定研究院颁发的《CAR-T 细胞治疗产品质量控制检测研究及非临床研究考虑要点》明确规定CAR 基因拷贝数 ⩽5 copies/细胞。另,在国内外法规中,对于VCN 的评价和要求日趋完善。
VCN 通常采用分子生物学手段例如qPCR 进行检测。设计CAR 目的片段的特异性引物探针,通过对细胞基因组提取,利用 qPCR 的方法,扩增目的基因片段,最终监测目的片段的拷贝数,以及内参基因的拷贝数,通过比值获得VCN 的结果,用以评价CART 的安全性。
2 平均载体拷贝数方法过程优化
2.1 方法概述
平均载体拷贝数方法,分为细胞基因组DNA 抽提,以及荧光定量 PCR 扩增两步骤。
细胞基因组DNA 抽提使用基因组抽提试剂盒,通过对细胞样本进行裂解,DNA 富集,过柱,洗脱,得到基因组DNA 样本。再通过对DNA 样本浓度测定,检测DNA 样本纯度、浓度,以识别DNA 样本的抽提质量。作为后续荧光定量PCR 扩增使用的模板。
荧光定量PCR 阶段,使用CAR 的目的片段以及内参基因设计的特异性引物、探针,以及DNA 扩增试剂盒,进行PCR 体系配制,然后加入抽提的DNA 样本作为扩增模板,经过特定程序扩增,获得CAR 目的片段的拷贝数以及内参基因的拷贝数。最终获得VCN 结果。
2.2 优化基因组DNA 抽提控制策略
(1)数据统计:汇总所有用于 VCN 检测的基因组DNA 抽提的结果,共计163 批。统计基因组DNA 的浓度,260nm 吸光值(A260)、260nm 和 280nm 的吸光值比值(A260/A280)、260nm 和 230nm 吸光值比值(A260/A230)以获得基因组DNA 纯度。
(2)数据分析
由上表可见,基因组 DNA 抽提浓度最低量为 24.157ng/μl,而 A260/A280 的浓度为 1.8~2.1 左右。对于后续CR 检测使用的模板 DNA 加入量的理论值为 100ng,即 50ng/μl 的基因组 DNA,加入 2μl。
通过对上述数据的分析,结合后续qPCR 扩增后的检验结果,对于原方法中100ng 的理论加入量,未进行实际探究,而当不满足理论加入量的样本检测结果,仍可能为合格结果。因此,后续探究该方法 qPCR 部分实际DNA 样品加入量,并通过验证证明方法的稳健性。
2.3 方法优化结论
基于上述基因组DNA 抽提结果,最低加入量的DNA 浓度为 24.157ng/μl,且后续qPCR 扩增结果良好,对VCN 的判定无影响。因此根据该统计数据,对方法进行DNA 加入量下探,以确定基因组 DNA 模板加入的最低量。同时对方法进行补充验证。
3 平均载体拷贝数方法验证
为探究及验证平均载体拷贝数基因组DNA 拷贝数最低加入量,基于上述结果,根据中国药典9101 分析方法验证指导原则,平均载体拷贝数方法属于含量测定中的定量方法,因此补充方法验证的内容检项包括线性范围、检测限、定量限及耐用性等几方面。
3.1 线性范围
(1)验证策略:该方法使用标准质粒,设计标准曲线,因此线性范围的验证浓度为标准曲线的浓度范围区间。基因 1 为 10~106 copies/μl,基因 2 的为 102~107 copies/μl,对该两项基因的区间分别进行验证,同时需满足精密度、准确度的要求。
(2)实验设计:线性范围的验证使用基因 1 和基因 2,采用连续稀释的方式,配制成6 个稀释度,即待验证稀释梯度 10~106 copies/μl 和 102~107 copies/μl,通过qPCR 扩增,计算基因1 和基因2 的标准曲线R2 值,需要满足标准曲线R2 值≥ 0.98;范围分析标准曲线各点检测结果,斜率满足-3.1~-3.8。
(3)实验操作:使用基因1 标准质粒制备 10~106 copies/μl,使用基因 2 标准质粒制备 102~107 copies/μl 稀释度。按照平均载体拷贝数的qPCR 方法,进行标准曲线的qPCR 检测。进行5 次独立实验(4)实验结果:
线性:标准曲线 R2 值=1.000范围:标曲各浓度点回收率结果如下表
表6 基因1 线性范围验证结果
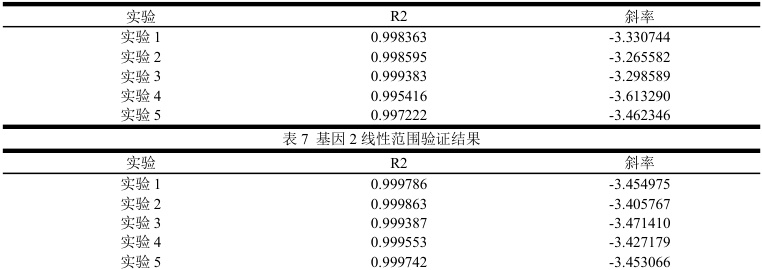
(5)实验结论:标准曲线的5 次独立实验线性R2 满足接受标准,斜率满足-3.1~-3.8,线性范围验证通过。3.2 检测限(1)验证策略:使用标准质粒基因1 和基因2,梯度稀释,对qPCR 的检测限进行验证,在95%的检出率应的最低浓度为该方法的检测限。
(2)实验设计:
使用基因 1 标准质粒,梯度稀释成 4 个浓度,即 1 copies/μl、5 copies/μl、10 copies/μl、20 copies/μl;使用基因 2 标准质粒,梯度稀释成 4 个梯度,即 40 copies/μl、20 copies/μl、10 copies/μl、5 copies/μl,进行 qPCR 扩增。每个浓度积累60 个孔的实验数据,检测限为至少57 个孔报阳的最低浓度。阴性的界定为仪器自身读数为未检出,或读数Ct 值 ⩾40 ,反之结果记为阳性。
(3)实验操作:
不同实验员,独立进行 3 次实验,每次使用每种基因的每个浓度,均进行20 个孔的复孔检测。(4)实验结果:检测限验证结果如下表
表7 基因1 检测限验证结果

(5)实验结论:
通过上述检测限验证结果,基因1 和基因 2 的检测限均为 5 copies/μl。
3.3 定量限
(1)验证策略:使用标准质粒基因 1 和基因2,梯度稀释,对qPCR 的检测限进行验证,满足精密度、准确度、回收率均满足的最低浓度为该方法的定量限。
(2)实验设计:
使用基因 1 标准质粒,梯度稀释成 7 个浓度,即 100 copies/μl、80 copies/μl 60 copies/μl、40 copies/μl、20copies/μl、10 copies/μl、5 copies/μl;使用基因 2 标准质粒,梯度稀释成 3 个梯度,即 100 copies/μl、50 copies/μl、25 copies/μl,进行 qPCR 扩增。独立进行3 次实验,每次实验每个浓度6 个复孔,共18 个复孔。复孔间 RSD% ⩽25% ,75%≤回收率 ⩽125% ,由高向低浓度依次判定,符合接受标准的最低浓度点为对应基因的检测限。
(3)实验操作:
不同实验员,独立进行 3 次实验,每次使用每种基因的每个浓度,均进行6 个孔的复孔检测。
(4)实验结果:定量限验证结果如下表
表7 基因1 定量限验证结果
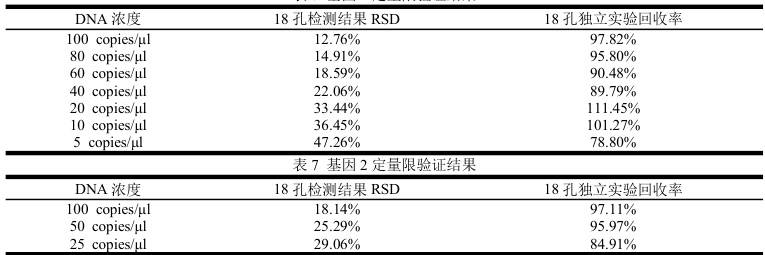
(5)实验结论:
通过上述定量限验证结果,基因 1 的定量限为 40 copies/μl,基因 2 的定量限为 100 copies/μl。
3.4 基因组 DNA 浓度下探
(1)验证策略:使用 3 批样品,分别使用不同基因组 DNA 浓度,按照平均载体拷贝数方法,进行qPCR扩增,检测基因1 和基因 2 的拷贝数,并计算VCN 结果。
(2)实验设计:
使用3 批样品,将抽提后的基因组 DNA 稀释为4 个浓度,分别为 60ng/μl 、 50ng/μl 、 40ng/μl 、 20ng/μl 。按照平均载体拷贝数方法,对基因 1 和基因2 进行扩增,检测2 种基因的拷贝数,并计算VCN 值,VCN 的RSD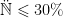 。
。
(3)实验操作:
使用3 批次样品,进行基因组DNA 抽提,抽提后 DNA 检测浓度,稀释成60 ng/μl、 50ng/μl 、40 ng/μl、20ng/μl 四个梯度,进行检测。
(4)实验结果:
表 8 3 批样品 VCN 结果

(5)实验结论:
通过对 4 个基因组DNA 浓度的验证,最低至 20ng/μl 加入量,其VCN 结果与 50ng/μl 的VCN 结果可比。
4 结论
通过对平均载体拷贝数的补充验证,探究了基因组 DNA 最低加入浓度为 20ng/μl ,同时qPCR 部分的补充验证可以支持这一结论。以确保在实际应用中,该方法能够真实且稳定反应CART 的平均载体拷贝数水平,以确保产品的安全性。
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)