从“奇偶”数字“看”基态原子中单电子的存在规律

徐江锋 陈炼
(浙江省春晖中学 绍兴市上虞区生态环境保护行政执法队,浙江 绍兴312300)
化学学科核心素养提出宏观辨识与微观探析,其蕴含着化学学科独有的认识视角和分析思路。提出的证据推理与模型认知是从学科观念和思维方式视角对化学学科思维的描述,要求学生形成化学学科的思想和方法。对于看不见、摸不着的原子核外电子,教师应采取哪些措施帮助学生将复杂、抽象的化学问题简单化,加深学生对化学知识的理解?又如何解决化学问题时锻炼学生逻辑推理能力,提升学生解决问题的能力,从而推动学生化学思维的发展?本文笔者从数字的角度辨析了原子序数奇偶性与其基态原子核外电子排布中单电子和成对电子的关系,以期帮助学生能更好的掌握构造原理及基态原子的电子排布规律。
规律一:原子序数为奇数的基态原子核外电子排布中一定存在单电子
泡利原理(也称泡利不相容原理)指出:在一个原子轨道里,最多只能容纳2 个电子,它们的自旋相反。其也表述为:基态原子中一定不存在2 个运动状态完全相同的电子。因此,依据泡利原理可知原子序数为奇数的基态原子核外电子排布中一定存在单电子。
规律二:原子序数为偶数的基态原子核外电子排布中可能存在单电子
洪特规则指出:基态原子中,填入简并轨道的电子总是先单独分占且自旋平行。另外,结合量子力学对原子轨道的定义:把电子在原子核外的一个空间运动状态称为一个原子轨道。根据量子力学的结论可知,无论哪个能级,其原子轨道数均为奇数。结合洪特规则,我们可以知道:原子序数为偶数的基态原子核外电子排布中可以存在单电子。下面列举第四周期元素加以说明。
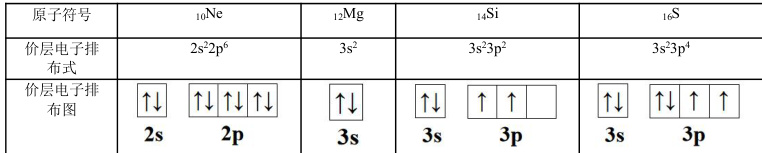
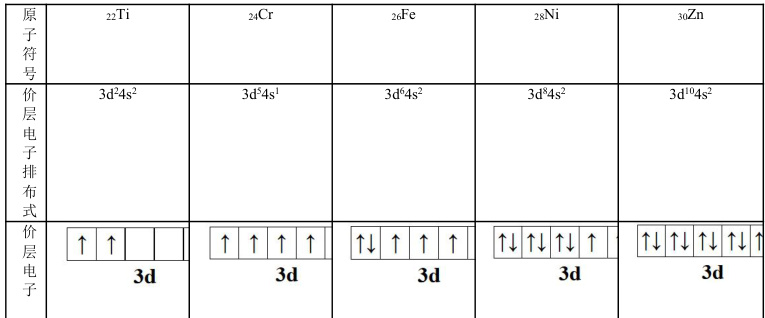

从以上前四周期偶数序数的原子价层电子排布式我们可以得出这样的规律:绝大多数原子核外均有单电子,除了各能级轨道上电子全充满的原子。这是因为各能级的轨道数为单数,电子在填充时又要尽可能多的占据能量相同的简并轨道,故只要各能级轨道电子未充满时一定存在单电子,且在轨道半充满时单电子的数量最多。
揭示规律本质:基态原子核外电子排布本质上要遵循能量最低原理
构造原理指出了基态核外电子填入能级的顺序,它是基于光谱学事实,是一个思维模型,其本质是能级能量的高低决定的。在一个多电子原子中,外层电子不仅受到原子核的吸引力,而且还要受到内层电子的排斥力。总体而言,外层电子受到核的吸引力会因内层电子而减弱,这就是屏蔽效应。这也就导致了原子核的核电荷数需要修正,即为有效核电荷数。因此,多电子原子中的一个电子的能量可借助斯莱特(Slater)规则并结合能量计算公式 E =− 13.6 × (Z−2σ e (公式中n 代表主量子数,Z 代表核电荷数,σ代表屏蔽常数,eV 是能量单位)得到。例如我们举周期表中唯一一个不满足规律二的原子——46Pd 原子为例,按照构造原理其价层电子排布式应为4d85s2,但实际的价层电子排布式确为 4d10 。我们可以假设 Pd 的最后一个电子填入 5s 能级,则可以依据上述计算公式得出该电子的近似能量 E5s=-6.86eVs 。同理,我们可以再次假设Pd 的最后一个电子填入4d 能级,计算出该电子的近似能量 E4d=. 39.88eV。通过计算证明 E4d5s ,所以钯原子中的最后一个电子填入 4d 轨道中时能量较低,导致偶数的原子序数不存在单电子。
另外,原子序数为偶数的基态原子核外存在单电子的原因还在于洪特规则。两个电子同占一个轨道时,电子间的排斥作用会使体系能量升高,只有分占等价轨道,才有利于降低体系的能量。该规则可利用电子自旋相关效应加以说明,其指出体系中自旋相同的电子对的总数越多,电子之间的总排斥能越小,体系的总能量就越低。所以在角量子数 l 相同的等价轨道上排布电子时应尽可能分占磁量子数m 值不同的轨道且自旋相同,以保证体系自旋相同的电子对的总数最多,以使体系的总能量最低。我们以 6C 原子为例说明,碳原子的基态核外电子排布式为 1s22s22p2,对于 2p 轨道上的 2 个电子有两种排布方式,一种为 1s22s22px2,另一种为 1s22s22px12py1。结合轨道表示式,可以两种排布方式中自旋相同的电子对数分别为6 对和7 对(如下图所示)。因此,后者排布时体系的能量最低,且必存在单电子。

综上所述,本文结合数学归纳探讨了原子序数奇偶性与原子核外电子排布中单电子出现的规律:若原子序数为奇数时基态原子的核外电子排布必 只要能级轨道未充满电子,基态原子的核外电子排布也必存在单电子。 特殊性的原因。通过本文的探讨,可以帮助学生更好的理解和运用基态原子核外电子排布的规律,也能为后续分子结构的学习打下扎实的基础。
参考文献
[1]宋天佑.无机化学(上册)[M].北京:高等教育出版社,2015:160.
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)